Τίτλος άρθρου: Αξιολόγηση τεχνολογιών υγείας και οφέλη από τη χρήση της
Όνομα συγγραφέα: ΜΕΝΤΗΣ ΙΣΙΔΩΡΟΣ
Ιδιότητα: Φαρμακοποιός (ΕΚΠΑ), Κάτοχος μεταπτυχιακού στη Σχολή Οικονομικών & Πολιτικών Επιστημών – Τμήμα Οικονομικών Επιστημών ΕΚΠΑ (Διοίκηση και Διαχείριση Οικονομικών Μονάδων & Οργανισμών με ειδίκευση «Οικονομικά της Υγείας και Διοίκηση Υπηρεσιών Υγείας»), Υποψήφιος Διδάκτωρ Ιατρικής Σχολής Αθηνών, στέλεχος του Τμήματος Παρακολούθησης & Αξιοποίησης Ελέγχων της Διεύθυνσης Φαρμάκου Κεντρικής Υπηρεσίας ΕΟΠΥΥ.*
*Οι απόψεις στο άρθρο είναι αμιγώς προσωπικές κατά την επιστημονική άποψη του συγγραφέα και δε δεσμεύουν τον ΕΟΠΥΥ.
Περίληψη
Το άρθρο στοχεύει στην αποτύπωση του προκύπτοντος οφέλους από τη χρήση της αξιολόγησης τεχνολογιών υγείας στη δημόσια υγεία, στο εγχώριο υγειονομικό σύστημα και την αξιοποίηση των αποτελεσμάτων της διεθνούς εμπειρίας, με παράλληλη κατάθεση μέτρων βελτιστοποίησης της σχετικής αξιολόγησης. Mέσω χρήσης βιβλιογραφίας και άντλησης άρθρων από σχετικές βάσεις δεδομένων, αναζητήθηκαν στοιχεία για την ιστορική διαδρομή και τα ισχύοντα δεδομένα της αξιολόγησης τεχνολογιών υγείας στον ελληνικό και ευρύτερο διεθνή χώρο και αναλύθηκαν διεξοδικά προκειμένου να καταστεί εφικτή η σύγκριση μεταξύ της διεθνούς εμπειρίας και της θεσπισθείσης εισαγωγής της αξιολόγησης τεχνολογίας υγείας στην Ελλάδα. Επιπρόσθετα, καταγράφηκε η αποτύπωση ομοιοτήτων και διαφορών μεταξύ των χαρακτηριστικών που προσδιορίζουν διεθνώς τις μεθόδους λειτουργίας φορέων αξιολόγησης τεχνολογιών υγείας και επιχειρήθηκε η εφαρμογή τους στα ελληνικά δεδομένα. Από τη σύγκριση της εφαρμογής της αξιολόγησης τεχνολογιών υγείας στην ημεδαπή με τη διεθνή εμπειρία, τεκμηριώθηκε η εναρμόνιση της πρώτης με τα ευρωπαϊκά δεδομένα και αποτυπώθηκαν τα αδιαμφισβήτητα οφέλη για όλους τους συντελεστές της λειτουργίας του ελληνικού υγειονομικού συστήματος καθώς και για τους ασθενείς, ως αποδέκτες των παρεχομένων υγειονομικών υπηρεσιών. Η αξιολόγηση των τεχνολογιών υγείας αποτελεί κρίσιμο παράγοντα για τη βιωσιμότητα και την αποτελεσματικότητα των διεθνών συστημάτων υγείας και συνεκδοχικά και του ελληνικού υγειονομικού συστήματος, εξοικονομώντας πολύτιμους πόρους. Παράλληλα, επισημάνθηκε και το πλήθος των προκλήσεων οι οποίες αναδύονται από την τεχνολογική πρόοδο που συντελείται στον χώρο της υγείας και κατατέθηκαν προτάσεις βελτιστοποίησης της εφαρμογής της αξιολόγησης νέων τεχνολογιών υγείας, προς επίτευξη της αναβάθμισης του επιπέδου υγείας των πολιτών.
Λέξεις ευρετηρίου: Αξιολόγηση τεχνολογίας υγείας, υγειονομικά συστήματα
Title of article: Health technology assessment and benefits from its use
Author: MENTIS ISIDOROS
Abstract
The article aims to capture the benefits from the use of health technology assessment in public health, in the domestic health system and the utilization of the outcomes of international experience, while certain measures should be applied for optimizing the health technology assessment. By using bibliography and retrieving articles from relevant databases, data were sought on the historical path and current application of health technology assessment in Greece and the wider international area and were thoroughly analyzed so as the comparison between international experience and introduction of health technology assessment in Greece could be feasible. Additionally, the identification of similarities and differences between the characteristics that internationally define the methods of health technology assessment bodies was recorded, attempting to apply them to the domestic health system. From comparison of the application of health technology assessment in Greece with international experience, the harmonization of the first with european data was documented as well as the indisputable benefits for all coefficients of the Greek health system and the patients, as users of the provided health services. The assessment of health technologies is crucial factor for the sustainability and efficiency of international health systems’ functioning and, by extent, of Greek health system’s, saving valuable resources. In parallel, numerous challenges arising from technological progress in health sector were highlighted and proposals were submitted to optimize the application of the evaluation of new health technologies, targeting to achieve the upgrading of citizens’ health level.
Key words: Health technology assessment, health systems
ΕΙΣΑΓΩΓΗ
Η υγειονομική περίθαλψη ως ανθρώπινο δικαίωμα κατοχυρώνεται στην οικουμενική διακήρυξη των ανθρωπίνων δικαιωμάτων και επαγωγικά αναπτύχθηκαν συστήματα υγείας, βάσει συγκεκριμένων αλληλεπιδρώντων στοιχείων, όπως εξασφάλιση χρηματοδότησης, διάθεση ανθρώπινων πόρων, διάχυση επιστημονικής πληροφόρησης, παροχή υπηρεσιών και εμβολίων καθώς και ανάπτυξη της ιατροτεχνολογικής βιομηχανίας. Η αδήριτη ανάγκη εφαρμογής αποτελεσματικών διατομεακών υγειονομικών πολιτικών, ερειδόμενες στα ανωτέρω στοιχεία, στοχεύει στην παροχή καθολικής υγειονομικής περίθαλψης (συμπεριλαμβανομένης πρόληψης-προαγωγής υγείας) και σε αξιολόγηση τεχνολογιών υγείας. Πυλώνας των βιώσιμων συστημάτων υγείας θεωρείται η πρόσβαση σε ανθρώπινο κεφάλαιο και αναλώσιμους πόρους, ενώ η διασφάλιση αυτών των εισροών απαιτεί οικονομικούς πόρους για φάρμακα, αναλώσιμο ιατροτεχνολογικό υλικό, μισθοδοσία υγειονομικού προσωπικού και επενδύσεις σε κτίρια-εξοπλισμό. Δεδομένων των περιορισμένων διαθεσίμων πόρων και του αυξανόμενου κόστους, η χάραξη υγειονομικής πολιτικής βασίζεται στη συγκράτηση του κόστους, σε αυξημένη χρηματοδότηση υπηρεσιών υγείας ή συνδυασμό αυτών.1 Τα υγειονομικά συστήματα αναπτύχθηκαν είτε βάσει μοντέλου Beveridge (χρηματοδότηση από κρατική φορολογία), είτε προτύπου Bismark (χρηματοδότηση από συστήματα κοινωνικής ασφάλισης με υποχρεωτικές εισφορές μισθωτών) είτε είναι μικτά (ελληνικό), στοχεύοντας σε παροχή ποιοτικών υπηρεσιών υγείας με τη μικρότερη δυνατή επένδυση πόρων, αντιμετωπίζοντας τις ίδιες προκλήσεις (προσδοκία χρήσης νέων τεχνολογιών υγείας, ραγδαία ανάπτυξη ιατροφαρμακευτικής τεχνολογίας, αυξανόμενο κόστος υπηρεσιών υγείας, δημογραφικό πρόβλημα-γήρανση πληθυσμού, προτεραιοποίηση επιλογών για ορισμό βέλτιστου μείγματος συμμετοχής στη δαπάνη κράτους-ασθενών, προσβασιμότητα-ποιότητα υπηρεσιών υγείας, περιορισμένοι πόροι). Το κυρίαρχο πρόβλημα είναι το αυξανόμενο κόστος υπηρεσιών υγείας και η αυξημένη ζήτηση χρήσης νέων τεχνολογιών υγείας, με την επιστημονική κοινότητα να καλείται να αποσαφηνίσει ποιες επιλογές είναι κατάλληλες.
ΑΞΙΟΛΟΓΗΣΗ ΤΕΧΝΟΛΟΓΙΑΣ ΥΓΕΙΑΣ (ΑΤΥ)
Ως τεχνολογία υγείας ορίζεται κάθε παρέμβαση δυνητικά χρησιμοποιούμενη για προαγωγή υγείας, πρόληψη/αποκατάσταση/θεραπεία/διαχείριση ασθενειών, συμπεριλαμβάνοντας φάρμακα, συσκευές, διαδικασίες και οργανωτικά συστήματα παροχής υγειονομικής περίθαλψης και η ΑΤΥ συνιστά διαδικασία ερωτήσεων-απαντήσεων για λήψη αποφάσεων χάραξης υγειονομικής πολιτικής, μέσω ανασκόπησης ιατρικών, κοινωνικοοικονομικών και δεοντολογικών επιπτώσεων της ανάπτυξης-χρήσης τεχνολογιών υγείας και των εκάστοτε δημόσιων υγειονομικών παρεμβάσεων. Συνεκδοχικά, υπολογίζεται ο αντίκτυπος στα εθνικά δημοσιονομικά δεδομένα, διευκολύνοντας τη λήψη αποφάσεων με συνεκτίμηση στοιχείων όπως κόστος, κίνδυνοι και οφέλη υφισταμένων-νέων τεχνολογιών και στοχεύοντας σε ενημέρωση (σε εθνικό-περιφερειακό-τοπικό επίπεδο) για θέματα προμήθειας και χρήσης τεχνολογίας υγείας, με αποτροπή επενδύσεων σε παρωχημένες είτε αναποτελεσματικές τεχνολογίες..2 Επίσης, η ΑΤΥ χρησιμοποιείται για καλύτερη κατανομή κόστους και αύξηση προσβασιμότητας ασθενών σε καινοτόμες θεραπείες, διασφαλίζοντας οφέλη για όλα τα ενδιαφερόμενα μέρη (stakeholders),3 με συμβολή στην προώθηση της καινοτομίας.4 Η οικονομική αξιολόγηση των τεχνολογιών υγείας και ο άμεσος/έμμεσος αντίκτυπος στα υγειονομικά συστήματα και στην υγεία των ασθενών είναι συνήθως μία μορφή κόστους-οφέλους, καταγράφουσα το κόστος σε χρηματικούς όρους, ενώ το όφελος αντανακλάται σε οικονομικούς όρους, κλινικούς (πχ. προσδόκιμο ζωής) ή ποιότητα ζωής. Ως εκ τούτου, για λήψη απόφασης χρήσης μιας τεχνολογίας απαιτείται καθορισμός τιμής-ποσοστού αποζημίωσης και οικονομική αξιολόγηση της προτεινόμενης υγειονομικής παρέμβασης (χορήγηση πιο αποτελεσματικού αλλά ακριβότερου φαρμάκου, επένδυση σε καινοτόμες τεχνικές, επιλογή εξοπλισμού, ίδρυση νέων υγειονομικών τμημάτων). Λόγω υψηλού κόστους απόκτησης-χρήσης της αξιολογούμενης τεχνολογίας υγείας και ταχείας εφαρμογής της, το κόστος φαρμάκων, εξοπλισμού και υγειονομικών εφαρμογών αυξάνεται, ενώ το οικονομικό αποτέλεσμα εξαρτάται από τον επιλεχθέντα τύπο αξιολόγησης (ένα νέο φάρμακο δύναται να κοστίζει περισσότερο, αλλά μπορεί να μειώνει έξοδα νοσηλείας/ημέρες άδειας από εργασία).5
Οι στόχοι είναι η ασφάλεια της τεχνολογίας (διαγνωστική-θεραπευτική) με αξιολόγηση πιθανών παρενεργειών, η αποτελεσματικότητα, η μέτρηση ικανότητας της νέας τεχνολογίας για επίτευξη των υποσχόμενων αποτελεσμάτων, η αποδοτικότητα (οικονομική αξιολόγηση), ο αντίκτυπος στην κοινωνία (δείκτης κόστους-αποτελεσματικότητας της νέας τεχνολογίας και ισότιμης πρόσβασης σε αυτήν), οι ηθικές παράμετροι της χρήσης και η διαθεσιμότητα των πληροφοριών.
Η ΑΤΥ απευθύνεται σε κέντρα λήψης αποφάσεων (κρατικές δομές-φορείς χάραξης πολιτικής υγείας), επαγγελματίες υγείας με έμφαση στους κλινικούς ιατρούς και κατ’ επέκταση στο σύνολο του ιατρικού κλάδου (για χρήση της επιλεχθείσης τεχνολογίας υγείας και εναρμόνιση με εκδοθείσες κατευθυντήριες οδηγίες), σε νοσοκομεία (επιλογή εξοπλισμού, παροχή υπηρεσιών), ιδιωτικές ασφάλειες υγείας (μορφή-εύρος ασφαλιστικής κάλυψης), ασθενείς–συλλόγους υπεράσπισης δικαιωμάτων τους (προσβασιμότητα σε υπηρεσίες υγείας, από κοινού με επαγγελματίες υγείας λήψη αποφάσεων), ακαδημαϊκή κοινότητα, ευρύ κοινό (πληροφόρηση για την προοπτική της παρεχομένης υγειονομικής παρέμβασης) και την ιατροφαρμακευτική βιομηχανία (για θέματα που άπτονται της παραγωγής-διάθεσης-εμπορίας ιατρικής τεχνολογίας), ενώ το σύστημα ΑΤΥ θα πρέπει να διασφαλίζει την ένταξη στις διαδικασίες και συμμετοχή όλων των ενδιαφερομένων.2
Το πλαίσιο έκδοσης κατευθυντήριων οδηγιών ΑΤΥ αφορά σε σαφείς διαδικασίες αξιολόγησης-λήψης αποφάσεων με περιθώρια ρεαλιστικών προσεγγίσεων, σύζευξη αξιολογήσεων κλινικής αποτελεσματικότητας με κοινωνικές αξίες, δημοσιονομικό αντίκτυπο, οικονομική αποτελεσματικότητα και ηθικές εκτιμήσεις του πληθυσμού στον οποίο απευθύνεται, αξιόπιστες-διαφανείς μεθόδους αξιολόγησης και διασφαλίζει τη συμμετοχή όλων των ενδιαφερομένων στις διαδικασίες (δίχως αποκλεισμό μεμονωμένων αποφάσεων χρηματοδότησης),6 με ενοποίηση πραγματικών δεδομένων προς ανάπτυξη διαρκώς καλύτερων διαδικασιών, για αναζήτηση μιας ευρέως αποδεκτής διαδικασίας ευχερέστερης πρόσβασης σε αποτελεσματικές νέες τεχνολογίες.7
ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΦΟΡΕΩΝ ΑΤΥ
Οι οργανισμοί ΑΤΥ υφίστανται κυρίως ως αυτόνομοι κρατικοί φορείς, με συμβουλευτική/ρυθμιστική λειτουργία. Συνήθως, μια τεχνική ομάδα αναλαμβάνει την αξιολόγηση των αποδεικτικών στοιχείων και μια έτερη ομάδα εμπειρογνωμόνων αξιολογεί την αίτηση ασφαλιστικής κάλυψης, υποβάλλοντας συστάσεις στο όργανο λήψης αποφάσεων. Οι περισσότεροι φορείς ΑΤΥ αξιολογούν κυρίως νέες ιατρικές τεχνολογίες, ακριβές ή/και με αβέβαια οφέλη. Τα κύρια αξιολογούμενα στοιχεία είναι: ο επιπολασμός-επιβάρυνση νόσου, θεραπευτικά αποτελέσματα-επιπτώσεις στην ασφάλεια, επίπεδο καινοτομίας, κοινωνικοοικονομικός αντίκτυπος, αποτελεσματικότητα και πηγές αποδεικτικών στοιχείων-κριτηρίων. Δεδομένου ότι οι νέες τεχνολογίες είναι ακριβότερες, οι διαθέσιμοι πόροι περιορισμένοι και κάθε νέα τεχνολογία υγείας δεν είναι απαραιτήτως και καινοτόμος, απαιτείται οικονομική αξιολόγηση από τους εντεταλμένους φορείς ΑΤΥ.
Οι μέθοδοι εξέτασης διαφέρουν βάσει μέτρησης αποτελεσμάτων, τεχνικής επεξεργασίας και προοπτικής και είναι αναλύσεις ελαχιστοποίησης κόστους (Cost Minimization Analysis-CMA), κόστους-αποτελεσματικότητας (Cost Effectiveness Analysis-CEA), κόστους-οφέλους (Cost Benefit Analysis-CBA) και κόστους-χρησιμότητας (Cost Utility Analysis-CUA), με το ποιοτικώς σταθμισμένο έτος ζωής (Quality Adjusted Life Year-QALY) προτιμώμενο μέτρο οικονομικής αξιολόγησης αξίας των υγειονομικών παρεμβάσεων (ένα QALY ισούται με έναν χρόνο τέλειας υγείας), με ενσωμάτωση πρόσθετων παραμέτρων στο σύστημα αποτίμησης. Η διαδικασία λήψης αποφάσεων βάσει μετρήσεων κόστους-αποτελεσματικότητας των οικονομικών αξιολογήσεων (πχ. κόστος ζωής/QALY) και αξιολόγησης της τρέχουσας αξίας των ιατρικών τεχνολογιών με οικονομική αξιολόγηση/συγκριτική αξιολόγηση κλινικών οφελών τελεί υπό διαρκή έλεγχο και με την ενίοτε αδυναμία καταγραφής της κοινωνικής αξίας της χρήσης να καταγράφεται ως περιορισμός. Επίσης και η διαφοροποιημένη (βάσει εκάστης μεθόδου αξιολόγησης) αποτύπωση της αξίας και η εθνική προτεραιοποίηση (λόγω διαφορετικών δημοσιονομικών περιορισμών-εθνικών προτεραιοτήτων) παράγουν συχνά διακρατική ετερογένεια αποφάσεων επιλογής φαρμάκων-αποζημίωσης και ζητήματα προσβασιμότητας (και κοινωνικής ισότητας) ασθενών στις νέες τεχνολογίες.
Άλλα χρησιμοποιούμενα στοιχεία περιλαμβάνουν αποδεκτές/προτιμώμενες πηγές δεδομένων, προσεγγίσεις συλλογής δεδομένων (απαίτηση συστηματικής βιβλιογραφίας) και σύνθεση δεδομένων (μετα-ανάλυση), ενώ τα κλινικά αποτελέσματα και η καταγραφή κόστους περιλαμβάνουν υπολογισμό του προεξοφλητικού επιτοκίου, συμπερίληψη των εκτιμώμενου χρονικού ορίζοντα χρήσης και συνεκτίμηση της ρητής/σιωπηρής προθυμίας πληρωμής για τη σχέση κόστους-αποτελεσματικότητας. Η εφαρμογή των αποτελεσμάτων περιλαμβάνει έκθεση αξιολόγησης σε δημόσια διαθεσιμότητα, πολιτικές συνέπειες εφαρμογής (τιμολόγηση-επιστροφή χρημάτων), τρόπο διάδοσης-εφαρμογής αποφάσεων, διαδικασίες προσφυγής-αναθεώρησης συστάσεων, ενώ διαφοροποιούνται βάσει χρηματοδότησης συστήματος υγείας (φορολογία-κοινωνική ασφάλιση), οργάνωσης (κεντρική-περιφερειακή), τύπου ΑΤΥ (οικονομική αξιολόγηση-κλινικό όφελος) και μέτρησης προοπτικής (για το υγειονομικό σύστημα και την κοινωνία).8 (Εικόνα 1)
Εικόνα 1: Διεκπεραίωση διαδικασιών ΑΤΥ
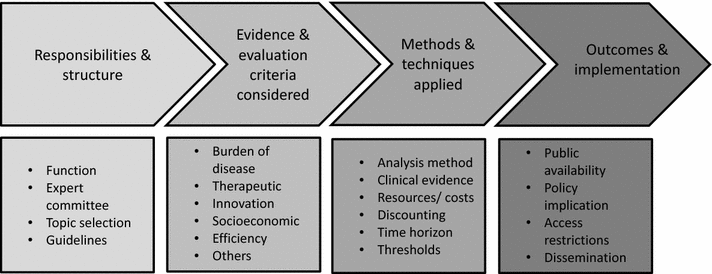
Πηγή: Angelis, Lange and Kanavos, 2018
ΕΥΡΩΠΑΪΚΗ ΔΙΑΔΡΟΜΗ ΑΤΥ
Η ΑΤΥ αναπτύχθηκε αρχικά στις ΗΠΑ (δεκαετία 1960) και επεκτάθηκε παγκοσμίως. Εισήχθη στην Ευρώπη με τη Σουηδία ως πρωτοπόρο (δεκαετία 1970) και τη Γαλλία, Ολλανδία και Αγγλία να ακολουθούν, με βαθμιαία αυξανόμενη χρήση επιστημονικών προτύπων ενσωμάτωσης τεχνολογιών υγείας στο υγειονομικό σύστημά τους. Εν συνεχεία, δημιουργήθηκαν οργανισμοί όπως ο Σουηδικός SPRI (1987), ο πρώτος εθνικός φορέας, κατόπιν άλλες ευρωπαϊκές χώρες (Γαλλία, Ισπανία) ίδρυσαν οργανισμούς (και περιφερειακώς σε Καταλονία, Ανδαλουσία, Μπασκόνια, Βαλένθια, Γαλικία, Μαδρίτη, 1990), ακολούθησαν η Σκωτία, Δανία, Φινλανδία, Γερμανία, Νορβηγία, Ελβετία, Αυστρία, Ουγγαρία και αργότερα η Ιρλανδία, το Βέλγιο, η Λετονία, η Πολωνία και η Ιταλία. Αρκετοί από τους πρώτους ευρωπαϊκούς οργανισμούς ήταν ιδρυτικά μέλη της INAHTA (1993). Το 1999 ιδρύθηκε ο NICE στην Αγγλία. Η συμμετοχή της Ευρωπαϊκής Επιτροπής κατέστη κρίσιμος παράγοντας για την προώθηση της ΑΤΥ. Επιπλέον, η Παγκόσμια Τράπεζα διαδραμάτισε βασικό ρόλο, ειδικά σε χώρες της Κεντρικής-Ανατολικής Ευρώπης και το 2003 ο Παγκόσμιος Οργανισμός Υγείας (ΠΟΥ) δημιούργησε το τεκμηριωμένο δίκτυο υγείας. Η Ευρωπαϊκή Επιτροπή ενίσχυσε τη συνεργασία των φορέων, υποστηρίζοντας (1993-2008) προγράμματα (EURASSESS-HTA EUROPE-ECHTA/ECAHI-EUnetHTA, στοχευόντων σε ανάπτυξη εργαλείων διακρατικής συνεργασίας, δημιουργία συντονιστικού μηχανισμού επικοινωνίας και σύνδεση δημόσιων εθνικών-περιφερειακών οργανισμών, ερευνητικών ινστιτούτων και υπουργείων υγείας, με κατάληξη τη δημιουργία ευρωπαϊκού δικτύου ΑΤΥ και διάδοση των αποτελεσμάτων στα κέντρα λήψης αποφάσεων των κρατών-μελών της Ευρωπαϊκής Ένωσης (ΕΕ).2
Τα ευρωπαϊκά δίκτυα ΑΤΥ είναι ο EMA, οργανισμός προώθησης της επιστημονικής αριστείας στην αξιολόγηση-εποπτεία φαρμάκων επ’ωφελεία της δημόσιας υγείας, το EUnetHTA, με αποστολή την ανάπτυξη οργανωτικού πλαισίου για ευρωπαϊκό δίκτυο έγκαιρης και αποτελεσματικής παραγωγής-μεταφοράς αποτελεσμάτων αξιολόγησης στα κράτη-μέλη της ΕΕ και τη σύνδεση εθνικών φορέων ΑΤΥ-ερευνητικών ινστιτούτων-υπουργείων υγείας επιτρέποντας ανταλλαγή πληροφόρησης-υποστήριξης αποφάσεων πολιτικής,7 η INAHTA, ο σημαντικότερος διεθνής οργανισμός ΑΤΥ, το ευρωπαϊκό παρατηρητήριο (European Observatory on Health Systems and Policies) που υποστηρίζει την ανάπτυξη πολιτικής υγείας βάσει ανάλυσης των ευρωπαϊκών συστημάτων υγείας, το διεθνές δίκτυο πληροφοριών για νέες και μεταβαλλόμενες τεχνολογίες υγείας (EuroScan) με συμβουλευτικό ρόλο, ως ευρωπαϊκό δίκτυο, ανταλλάσσοντας πληροφορίες για νέα φάρμακα, συσκευές και σχετικές διαδικασίες και το HEN, πηγή δεδομένων με αποστολή την οικοδόμηση πολιτικής υγείας με ταχεία πρόσβαση σε αξιόπιστες πληροφορίες στοιχείων υγείας.
Σχετικά με τους εθνικούς φορείς ΑΤΥ, το NICE, ανεξάρτητος φορέας, αποτελεί σημείο αναφοράς, παρέχοντας καθοδήγηση σε νέες τεχνολογίες θεραπείας ασθενειών και στοχεύοντας στη δημιουργία διαφανούς διαδικασίας προσδιορισμού του βαθμού κλινικής αποτελεσματικότητας της υπό αξιολόγηση θεραπείας συγκριτικά με το επαγόμενο κόστος στο εθνικό υγειονομικό σύστημα (NHS). Οι αξιολογήσεις διεξάγονται από ανεξάρτητη επιτροπή αξιολόγησης στελεχωμένη από το NHS, ομάδες ασθενών, ακαδημαϊκή κοινότητα και την ιατροφαρμακευτική βιομηχανία. Ενώ οι συστάσεις δεν έχουν θεσμικό βάρος, το NHS υποχρεούται να τις εφαρμόσει ενώ ο αντίκτυπός τους είναι σημαίνων και εκτός του Ηνωμένου Βασιλείου.
Επιπροσθέτως, το IQWIG, γερμανικό ανεξάρτητο επιστημονικό ινστιτούτο ΑΤΥ, αξιολογεί την αποτελεσματικότητα των υγειονομικών παρεμβάσεων για επιλεγμένες ασθένειες, τα οφέλη και το κόστος φαρμάκων, παρέχει πληροφορίες στους ασθενείς και το ευρύ κοινό και εκδίδει κατευθυντήριες γραμμές. Το χρησιμοποιούμενο κριτήριο είναι η θεραπευτική υπεροχή έναντι υφισταμένων θεραπειών.9 Στο έργο του φορέα συμμετέχουν ισότιμα η ομοσπονδιακή κυβέρνηση και τα ασφαλιστικά ταμεία υγείας (περιλαμβάνοντα ιατρούς, νοσοκομεία, οργανώσεις πολιτών) και οι εκδιδόμενες οδηγίες στηρίζονται σε τεκμηριωμένα ιατρικά κριτήρια. Πρόσβαση στη θεραπεία έχουν όλοι οι ασφαλισμένοι, ενώ θα πρέπει να αποδεικνύεται η ιατρική αναγκαιότητα της υπό αξιολόγηση υγειονομικής παρέμβασης (το αποδεδειγμένο όφελος να είναι σημαντικό με την παρέμβαση ως τον μόνο τρόπος επίτευξής του). Για τη μεθοδολογία προσδιορισμού οφέλους, αξιολογούνται η βελτίωση κατάστασης υγείας, η μείωση διάρκειας νόσου, η παράταση-βελτίωση ποιότητας ζωής και αρνητικά στοιχεία (θνησιμότητα-νοσηρότητα). Το IQWiG αποφασίζει επίσης για την τιμή καινοτόμων φαρμάκων (βάσει πρόσθετου θεραπευτικού οφέλους) και εφαρμογή διεθνώς αποδεκτών ιατρικών προτύπων προσαρμοσμένη στις εθνικές απαιτήσεις.10
Τέλος, η Haute Autorité de Santé (HAS), ανεξάρτητος φορέας και συμβουλευτικό όργανο για τις γαλλικές δημόσιες αρχές, αξιολογεί τις βέλτιστες πρακτικές υγειονομικής περίθαλψης, τη διαπίστευση οργανισμών υγειονομικής περίθαλψης, τα αναμενόμενα-πραγματικά κλινικά οφέλη (φαρμάκων, ιατροτεχνολογικών προϊόντων, διαγνωστικών-θεραπευτικών διαδικασιών, υφισταμένης τεχνολογίας υγείας), τη βελτίωση της ιατρικής πρακτικής, την πιστοποίηση ιατρών, μεριμνώντας για τη διάδοση ιατρικών πληροφοριών σε ασθενείς καθώς και την ανάπτυξη κατευθυντήριων γραμμών ορθής πρακτικής και προγραμμάτων διαχείρισης χρόνιων ασθενειών. Το ιατρικό πλεονέκτημα (Εικόνα2) αξιολογείται ανά ιατρική υπηρεσία/προϊόν, αξιολογώντας τη σοβαρότητα της διάγνωσης και τα δεδομένα χρήσης φαρμάκου για συγκεκριμένη ένδειξη, με τροποποιημένη αξιολόγηση, όταν παράγονται νέα δεδομένα/πιο αποτελεσματικές εναλλακτικές λύσεις.8
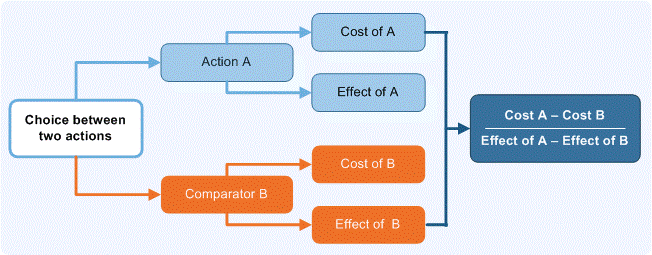
Εικόνα 2: Συγκριτική αποτελεσματικότητα χρήσης τεχνολογίας υγείας στη Γαλλία
Πηγή: www.has-sante.fr/portail/jcms/c_2035665/en/methods-for-health-economic-evaluation
Παρά τη διαφοροποίηση των χαρακτηριστικών-διαδικασιών των φορέων ΑΤΥ, αναγνωρίζεται ένα σύνολο κοινών σημείων για τον αντίκτυπο στην κοινωνία, τις επιπτώσεις στη δημόσια υγεία, την πρόσβαση στην περίθαλψη, την καινοτομία και τη βιωσιμότητα της δημόσιας χρηματοδότησης της υγειονομικής περίθαλψης.
Οι φορείς ΑΤΥ διαφέρουν ως προς τη δομή, συχνά διαφέρουν στις πρακτικές που ακολουθούνται και στην αξιολόγηση (τελικά σημεία, τρόπος ενσωμάτωσης, σημασία), στην ερμηνεία και προτεραιοποίησή τους (υποκειμενικότητα επιλογής κριτηρίων), στη διασφάλιση διαφάνειας, στη στόχευση στους αποδέκτες των παρεμβάσεων τους και την αλληλεπίδραση με τις εθνικές αρχές αποζημίωσης. Ορισμένες βορειοευρωπαϊκές χώρες (Ολλανδία, Σουηδία, Αγγλία) προτιμούν την προσαρμογή κόστους ανά σταθμισμένα όρια προσδόκιμου ζωής, σε αντίθεση με τις χώρες της κεντρικής-νότιας Ευρώπης. Ωστόσο, τα γενικά χαρακτηριστικά του ευρωπαϊκού μοντέλου είναι ορατά. Εκτός από τη συγκριτική αξιολόγηση του κλινικού οφέλους, οι περισσότερες χώρες εφαρμόζουν έναν τύπο οικονομικής αξιολόγησης (κυρίως CUA/CEA) και το QALY είναι το προκρινόμενο μέτρο. Το αποτέλεσμα χρησιμοποιείται για συστάσεις αποζημίωσης ιατρικής τεχνολογίας υπό μορφή οδηγιών. Συνεκτιμώντας τη σχέση κόστους-αποτελεσματικότητας, ορισμένες χώρες (Αγγλία, Ολλανδία) έχουν καθιερώσει διαδικασίες υπολογισμού κόστους-αποτελεσματικότητας, ενώ άλλες (Γαλλία) δεν ενσωματώνουν επίσημα χρηματοοικονομικά στοιχεία.7 Δεδομένου ότι κανένα μοντέλο ΑΤΥ δεν είναι καθολικά εφαρμόσιμο-πλήρως αποδεκτό, οι διαδικασίες πρέπει να προσαρμόζονται στις ανάγκες κάθε χώρας, βάσει χαρακτηριστικών εκάστης (μορφή υγειονομικού συστήματος, εύρος πληθυσμού, διοικητικές δομές, διαθέσιμοι πόροι).
ΘΕΣΠΙΣΗ ΑΤΥ ΣΤΗΝ ΕΛΛΑΔΑ
Το ελληνικό υγειονομικό σύστημα είναι μεικτό, με εφαρμογή κοινωνικής ασφάλισης (υπό κρατική χρηματοδότηση μέσω δημόσιων πόρων, προϋπολογισμού, ασφαλιστικών εισφορών και ιδιωτικών πληρωμών) και καθολικής πρόσβασης στις υγειονομικές υπηρεσίες. Το 1983 καταγράφηκε μεταρρύθμιση της υγειονομικής περίθαλψης, βάσει προτύπου Bismarck για την κοινωνική ασφάλιση, υπό την αιγίδα της κρατικής χρηματοδότησης και στοχεύοντας στη μείωση του ιδιωτικού τομέα και την καθολική υγειονομική κάλυψη. Όμως, η υγειονομική περίθαλψη παρέμενε ασυντόνιστη, ενώ οι πληρωμές καθορίζονταν κυρίως από ιδιωτικές δαπάνες, με τις υπηρεσίες υγείας να καλύπτονται από την κοινωνική ασφάλιση δίχως συνεκτίμηση σχέσης κόστους-αποτελεσματικότητας. Το υγειονομικό σύστημα χαρακτηρίστηκε από ανισότητες, γραφειοκρατία, αλόγιστη χρήση νοσοκομειακών κλινών, έλλειψη οικονομικής αποδοτικότητας ενώ εισήχθησαν τεχνολογίες υγείας άνευ διερεύνησης υφισταμένων αναγκών. Ωστόσο, η διεθνής προώθηση της ΑΤΥ ώθησε τη χώρα στη συμμετοχή της σε σχετικά ευρωπαϊκά προγράμματα.11 Μέχρι πρόσφατα, η Ελλάδα και ορισμένες άλλες χώρες αποτελούσαν εξαίρεση, δίχως θεσμοθέτηση ΑΤΥ, παρά το ότι οι αποσπασματικές δράσεις (ίδρυση Εθνικού Κέντρου Αξιολόγησης της Ποιότητας και Τεχνολογίας στην Υγεία-ΕΚΑΠΤΥ) είχαν αναδείξει τη σημασία των ευεργετικών αποτελεσμάτων της αξιολόγησης (παροχή υπηρεσιών υγείας υψηλής ποιότητας, πρόληψη διασπάθισης πόρων).12
Η παλαιότερη νομοθεσία (ΦΕΚ 2912/2012) επικαιροποιήθηκε (Ν.4512/2018, άρ.247-256, Ν.4633, Ν.4633/2019,άρ 22) και με τον Ν.4512/2018 (άρθρο 247), συστάθηκε επιτροπή αξιολόγησης και αποζημίωσης φαρμάκων, με έργο την έκδοση γνωμοδότησης στον υπουργό υγείας, κατόπιν αξιολόγησης των φαρμάκων που έχουν λάβει άδεια κυκλοφορίας και κυκλοφορούν στην Ελλάδα, για ένταξη/από-ένταξή τους από τον θετικό κατάλογο (Κατάλογος Αποζημιούμενων Φαρμάκων-ΚΑΦ) και την αναθεώρηση του. Με τα άρθρα 248-254 ορίσθηκαν η σύνθεση, ο ορισμός μελών της επιτροπής, τα κριτήρια, η μεθοδολογία αξιολόγησης, η διαδικασία αξιολόγησης, η αναθεώρηση και κατάρτιση του ΚΑΦ, η αρχή αμεροληψίας, τα ασυμβίβαστα μελών, τα καθήκοντα εχεμύθειας και η ευθύνη μελών. Επίσης, με το άρθρο 254 συστάθηκε επιτροπή διαπραγμάτευσης τιμών φαρμάκων υπαγόμενη στον υπουργό υγείας, με αρμοδιότητα να διαπραγματεύεται τιμές/εκπτώσεις φαρμάκων που αποζημιώνονται από τον Εθνικό Οργανισμό Παροχής Υπηρεσιών Υγείας (ΕΟΠΥΥ) ή προμηθεύονται τα δημόσια νοσοκομεία, να συνάπτει συμφωνίες με τους κατόχους αδειών κυκλοφορίας (ΚΑΚ) που συμμετέχουν στη διαδικασία διαπραγμάτευσης και να εισηγείται στην επιτροπή αξιολόγησης για την επίπτωση της αποζημίωσης των φαρμάκων στον εθνικό προϋπολογισμό. Παράλληλα, με το άρθρο 255 συστάθηκε στον ΕΟΠΥΥ επιτροπή διαπραγμάτευσης αμοιβών και τιμών ιατροτεχνολογικών προϊόντων, προκειμένου να διαπραγματεύεται με τους συμβαλλομένους παρόχους τις αμοιβές τους, τους όρους συμβάσεων του ΕΟΠΥΥ και τις τιμές ιατροτεχνολογικών υλικών, καθώς και να εισηγείται στο διοικητικό συμβούλιο του ΕΟΠΥΥ τη διατήρηση/τροποποίηση των ανωτέρω. Παρά το ότι δεν υπήρξε νομοθετική πρόβλεψη για υπολογισμό του έμμεσου κόστους και ηθικών παραμέτρων, με τη θεσμική εισαγωγή ΑΤΥ, ως ορόσημο για τη χώρα, τα γενικά χαρακτηριστικά του ευρωπαϊκού μοντέλου καθίστανται ευδιάκριτα και με αξιοποίηση των διεθνών ευρημάτων, η χώρα επωφελείται από τη μεταφορά αποτελεσμάτων.
ΠΡΟΚΛΗΣΕΙΣ ΚΑΙ ΕΘΝΙΚΕΣ ΠΡΟΟΠΤΙΚΕΣ ΑΠΟ ΤΗΝ ΕΦΑΡΜΟΓΗ ΑΤΥ
Η ΑΤΥ, διεπιστημονικός πυλώνας πολιτικής υγείας, συμβάλλει σε εξοικονόμηση πόρων και αποτελεσματικότερη θεραπεία ασθενών, εντοπίζοντας τις λιγότερο αποτελεσματικές τεχνολογίες υγείας και συνιστά την απάντηση στο αυξανόμενο κόστος υγείας.12 Πρέπει επίσης να τονιστεί η αναγκαιότητα εναρμόνισης των κρατών-μελών της ΕΕ (συμπεριλαμβανομένης της Ελλάδας) με την αρχή της επικουρικότητας για διαχείριση της ανομοιογένειας συστάσεων με συνεργατική αξιολόγηση από άλλα κράτη και διαμοιρασμό πληροφοριών και ευθυγράμμιση χρόνου έγκρισης τεχνολογιών υγείας. Τα αποδεκτά (από όλα τα κράτη-μέλη) κριτήρια πρέπει να είναι σαφή και ενσωματωμένα στη διαδικασία αξιολόγησης προς αντιμετώπιση της ετερογένειας συστάσεων, παρέχοντας ευελιξία στην απόφαση ασφαλιστικής κάλυψης τεχνολογίας υγείας.8 Αναφορικά με τη διαφάνεια, υπογραμμίζεται η σημασία της αναγκαιότητας οικοδόμησης κλίματος εμπιστοσύνης και αγαστής επικοινωνίας μεταξύ των φορέων ΑΤΥ και των αξιολογούμενων εταιρειών, προς αντιμετώπιση της αμοιβαίας δυσπιστίας αποδοχής διαδικασιών-αποδεικτικών στοιχείων και άμβλυνση των διαφορών που συνοψίζονται στους εταιρικούς ισχυρισμούς (τα αξιολογούμενα στοιχεία αποτελούν μόνο μέσο περιορισμού κόστους, οι φορείς ΑΤΥ ενδιαφέρονται μόνο για τυχαιοποιημένες ελεγχόμενες δοκιμές -Randomized Controlled Trials-RCTs, η απουσία αποδεικτικών στοιχείων δε συνεπάγεται αναξιοπιστία προϊόντος, οι φορείς ΑΤΥ εφαρμόζουν αδιαφανείς διαδικασίες, αγνοώντας τα μοντέλα αξιολόγησης που χρησιμοποιούν οι εταιρείες) και τους ισχυρισμούς φορέων ΑΤΥ (εστίαση εταιρειών στην αξία με αγνόηση του κόστους, αμφισβήτηση των υποβληθέντων δεδομένων, έλλειψη εμπιστοσύνης στα μοντέλα αξιολόγησης που χρησιμοποιούνται από τις εταιρείες, απουσία διαφάνειας). Για την ενσωμάτωση πραγματικών δεδομένων, η διεθνής ιατρική κοινότητα αναγνωρίζει ότι τα RCTs έχουν περιορισμένη γενικευσιμότητα και στερούνται ακρίβειας, ενώ επιχειρείται η αναζήτηση προηγμένων μεθόδων σύνθεσης κλινικών δεδομένων με παράλληλη μέτρηση αξίας και σχέσης κόστους-αποτελεσματικότητας. Ακόμη, συνιστώνται ανεξάρτητες αξιολογήσεις, πολύπλευρες στρατηγικές πληροφόρησης και χρήση ηλεκτρονικών αρχείων ασθενών.13
Δεδομένου ότι, έως σήμερα, η Ελλάδα χρησιμοποιεί τα αποτελέσματα ΑΤΥ άλλων χωρών, η εγχώρια θεσμική εισαγωγή ΑΤΥ προκρίνει τη συνεχή εκπαίδευση του επιστημονικού δυναμικού του φορέα ΑΤΥ, τη σύνδεση ΑΤΥ και ιατρικής βασιζόμενη σε στοιχεία (Evidence-Based Medicine-EBM, ήτοι συνδυασμός της κλινικής εμπειρίας επαγγελματιών υγείας βάσει συστηματικής συλλογής-ανάλυσης κλινικών δεδομένων με προτεραιότητες του ασθενούς για έκδοση εξατομικευμένων ανά ασθενή ιατρικών οδηγιών), τη διαρκή βελτίωση διαδικασιών παρακολούθησης, υποβολής εκθέσεων, αξιολόγησης, ενημέρωσης προϋπολογισμού-αναθεώρησης και επένδυσης σε οικονομικούς-ανθρώπινους πόρους, τον διαχωρισμό κατευθυντηρίων οδηγιών (μεμονωμένες περιπτώσεις έναντι όσων απευθύνονται σε ομάδες ασθενών καθορισθείσες με κλινικά κριτήρια), τη βελτίωση μεθόδων δεδομένων (χρήση πολλαπλών μεθόδων αξιολόγησης), τη διεύρυνση του υπό μελέτη πληθυσμού (ώστε το εύρος να ανταποκρίνεται στις απαιτήσεις των αξιολογήσεων), την ευχερή πρόσβαση στα δεδομένα (για εξασφάλιση της διαφάνειας κριτηρίων αξιολόγησης-αποδεικτικών στοιχείων-αποφάσεων-σύνθεσης επιτροπών αξιολογήσεων), την εξέταση του κοινωνικο-δεοντολογικού πλαισίου και συμμετοχή όλων των φορέων9.
Η Ελλάδα οφείλει να αδράξει την ευκαιρία, καθορίζοντας στόχους, πλαίσιο, μεθόδους και συμμετέχοντες (και τον ρόλο τους) σε διαδικασίες με την αρωγή του εγκατεστημένου συστήματος ηλεκτρονικής συνταγογράφησης (ΣΗΣ) και την αποσαφήνιση του κοινωνικού αντίκτυπου της ΑΤΥ. Προτείνεται η επικέντρωση στις μεθόδους μέτρησης κλινικής προστιθέμενης αξίας και στον αντίκτυπο στον εθνικό προϋπολογισμό, με ευρεία χρήση αναλύσεων πολλαπλών κριτηρίων CBA/ ευρύτερων αναλύσεων, ως πιο σαφείς-διαφανείς. Όπου απουσιάζουν τα RCTs, η Ελλάδα θα μπορούσε να επωφεληθεί από το εκτεταμένο ΣΗΣ που περιέχει εξατομικευμένες πληροφορίες για ασθενείς, ηλικία, φύλο, ICD-10, δραστικές ουσίες, εμπορικές ονομασίες και ποσότητες Ταυτόχρονα, απαιτείται η χαρτογράφηση των διαθέσιμων ανθρώπινων πόρων (επαγγελματίες υγείας, ακαδημαϊκοί, φορείς ασθενών) για ανάλυση αποφάσεων-αξιολόγηση-υλοποίηση και ανάπτυξη κλινικών κατευθυντήριων οδηγιών, η κινητροδότηση του προσωπικού που συμμετέχει στις διαδικασίες, ο σχεδιασμός ειδικού προϋπολογισμού, η ακριβής πρόβλεψη και βέλτιστη κατανομή των απαιτούμενων εκπαιδευτικών-τεχνικών πόρων και η επιστημονική τεκμηρίωση αποφάσεων. Η ανάπτυξη κατευθυντηρίων οδηγιών διεξαγωγής φαρμακοοικονομικής αξιολόγησης, η αλλαγή στόχευσης της πολιτικής υγείας, η καταγραφή δαπανών-επιδημιολογικών δεδομένων και η ευρύτερη συμμετοχή των ενδιαφερομένων στις διαδικασίες λήψης αποφάσεων θεωρούνται προϋπόθεση επιτυχούς εφαρμογής της εγχώριας ΑΤΥ,14 με τήρηση του νομικού πλαισίου και επαρκή χρηματοδότηση του φορέα. Έτσι, αποτρέπονται επενδύσεις σε απαρχαιωμένες/αναποτελεσματικές τεχνολογίες και υποστηρίζονται καινοτόμες δράσεις (πχ. διάδοση ποιοτικών γενοσήμων φαρμάκων, προς όφελος καταναλωτών και εθνικών υγειονομικών συστημάτων).15Επιπλέον, η Ελλάδα, συμμετέχοντας σε κοινές δράσεις φορέων ΑΤΥ, θα μπορούσε να επωφεληθεί από τη δυνατότητα μεταφοράς αποτελεσμάτων από κοινές πρωτοβουλίες της ΕΕ.16 Η συνεργασία μεταξύ χωρών είναι ζωτικής σημασίας για ενίσχυση της ΑΤΥ σε αναδυόμενες προκλήσεις,17 όπως η πρόσφατη πανδημία Covid-19, αναδεικνύοντας την ανάγκη ενισχυμένης διεθνούς συνεργασίας.18 Πρόσθετα, εκδηλώνεται ενδιαφέρον για συμμετοχή ασθενών στις διαδικασίες ΑΤΥ. Η Ευρωπαϊκή Επιτροπή πρότεινε πλαίσιο ευρωπαϊκής συνεργασίας ΑΤΥ και διεξαγωγής κοινών κλινικών αξιολογήσεων, όπου αναφέρεται η συμμετοχή ασθενών, προσφέροντας δυνατότητα διασυνοριακής συνεργασίας, ανάπτυξης και συμμετοχής ασθενών στην ευρωπαϊκή ΑΤΥ. Η δημιουργία πολυμερούς ομάδας ΑΤΥ της ΕΕ για ενθάρρυνση της συμμετοχής ασθενών στις δράσεις της ΑΤΥ είναι βαρύνουσας σημασίας για τη συνεκδοχική ανάπτυξη της ευρωπαϊκής ΑΤΥ.19 Επίσης, η συνεργασία των κρατών-μελών θα πρέπει να υποστηρίζεται σθεναρά από την Ευρωπαϊκή Επιτροπή.20 Η τελευταία, την 01/2018, δημοσίευσε πρόταση κανονισμού για την ΑΤΥ, η οποία έκτοτε συζητήθηκε εκτενώς, όμως εξακολουθούν να υφίστανται αποκλίνουσες θέσεις (το Ευρωπαϊκό Κοινοβούλιο πρότεινε συστάσεις για τροπολογίες).21 Παρά τα αρχικά θετικά αποτελέσματα της διεθνούς συνεργασίας, μελλοντικά θα πρέπει να αποδειχθεί ότι μπορούν να ξεπεραστούν τα υφιστάμενα εμπόδια (πχ. νομοθετικές απαιτήσεις).22 Επιπρόσθετα, δημοσιευμένα άρθρα και μελλοντικές προτάσεις έργων από το EUnetHTA συνεπικουρούν τους ευρωπαϊκούς φορείς ΑΤΥ προς επίτευξη συνεργασίας, προκειμένου να ευθυγραμμιστούν οι πολιτικές με τα δεδομένα πραγματικού κόσμου και να καταστεί δυνατή η αποτελεσματική χρήση τους στη διαδικασία λήψης αποφάσεων,23 ενώ η ενδεχόμενη ίδρυση ενιαίου ευρωπαϊκού φορέα ΑΤΥ με εναρμόνιση θεμελιωδών στοιχείων (κατευθυντήριες οδηγίες οικονομικής αξιολόγησης, διαδικασίες λήψης απόφασης, κοινωνική προθυμία πληρωμής για τεχνολογίες υγείας) θα καταστεί χρήσιμο εργαλείο αντιμετώπισης της διαφοροποίησης των πρακτικών ΑΤΥ.24 Με την τελευταία, ως συστηματική αξιολόγηση ιδιοτήτων και επιπτώσεων μιας τεχνολογίας υγείας (για εκτίμηση άμεσων-επιδιωκόμενων επιπτώσεων και έμμεσων-ακούσιων συνεπειών της)20 και ως πολυεπιστημονικό πεδίο δράσης κυβερνήσεων, υγειονομικών συστημάτων, φορέων χάραξης πολιτικής, επαγγελματιών υγείας, δημόσιων-ιδιωτικών οργανισμών και ασθενών (Εικόνα 3), εξοικονομούσα χρόνο και πόρους στο σύστημα υγείας και παρέχοντας υψηλό επίπεδο υγειονομικής περίθαλψης12 και βασικό άξονα της κοινής ευρωπαϊκής φαρμακευτικής πολιτικής, θα πρέπει να προτεραιοποιηθεί σε ευρωπαϊκό επίπεδο η αξιολόγηση της προστιθέμενης θεραπευτικής αξίας νέων φαρμακευτικών θεραπειών, καλύπτοντας το κενό των κλινικών αποδεικτικών στοιχείων για έγκριση και αποζημίωση φαρμάκων σε όλες τις χώρες, περιορίζοντας τις εγχώριες διαπραγματεύσεις τιμολόγησης και επίδρασης στον προϋπολογισμό.25 Η εγχώρια εφαρμογή ΑΤΥ προσφέρει πολλαπλά οφέλη για τον ασθενή, με τη διάχυση-εφαρμογή αποτελεσματικών τεχνολογιών υγείας να συνιστά το μακροπρόθεσμο όφελος για το σύστημα υγείας, με εξοικονόμηση πολύτιμων πόρων, ενώ η επίτευξη του στόχου απαιτεί επένδυση χρόνου, προσωπικού, οικονομικών πόρων και ευρεία αποδοχή της θεσπισθείσης διαδικασίας ΑΤΥ.26
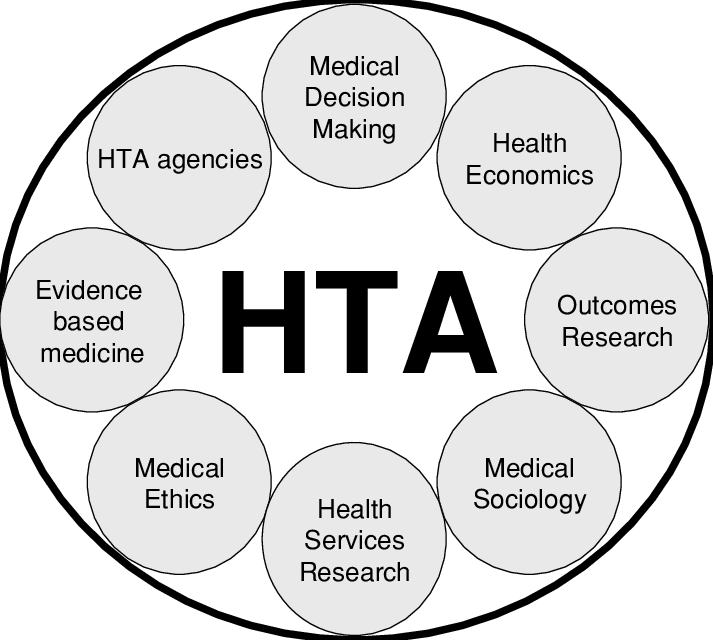
Εικόνα 3 Η αξιολόγηση τεχνολογίας υγείας ως πολυεπιστημονικό πεδίο
ΕΠΙΔΡΑΣΗ ΤΗΣ ΑΤΥ ΣΤΟΥΣ ΔΕΙΚΤΕΣ ΥΓΕΙΑΣ
Ιδιαίτερης μνείας χρήζει η αξιολόγηση των επιπτώσεων των παραγομένων αποτελεσμάτων ΑΤΥ επί των δεικτών υγείας που διαχωρίζονται σε θετικούς (προσδόκιμο ζωής, ποσοστό γεννήσεων-γονιμότητας), αρνητικούς-σχετικούς με εμφάνιση νόσων-παθολογικών καταστάσεων (δείκτης νοσηρότητας, ποσοστό θνησιμότητας), οικονομικούς- διοικητικούς δείκτες (δαπάνες υγείας ως % ΑΕΠ, κατά κεφαλήν δαπάνες υγείας, αριθμός ιατρών, νοσηλευτικό προσωπικό, νοσοκομειακές κλίνες, νοσοκομειακές εισαγωγές/εξιτήρια, μέση διάρκεια παραμονής, επισκέψεις εξωτερικών ασθενών-εργαστηριακές εξετάσεις, μέσος όρος πληρότητας κλινών), έτη υγιούς ζωής, δυνητικά απολεσθέντα έτη ζωής, ποιοτικά σταθμισμένα έτη, προσδόκιμο υγιούς ζωής και σταθμισμένα ως προς αναπηρία έτη ζωής. Επισημαίνεται ότι η θνησιμότητα σχετίζεται και με κοινωνικοοικονομικές επιπτώσεις βάσει φύλου, ηλικίας, τόπου διαμονής, οικογενειακής κατάστασης, συνθηκών υγειονομικής περίθαλψης, επιβλαβών συνηθειών (κάπνισμα, κατανάλωση αλκοόλ), διατροφής, κληρονομικότητας και επαγωγικά συνδέεται με την οικονομική ανάπτυξη-βελτιωμένες συνθήκες διαβίωσης, βελτίωση υπηρεσιών υγείας και διάδοση τεχνολογίας. Η βρεφική θνησιμότητα αντανακλά την κατάσταση της υγείας ενός πληθυσμού και πολλοί δείκτες συνδυάζονται με δημογραφικά στοιχεία (βρεφική-νεογνική θνησιμότητα, θάνατοι ως απόρροια χρόνιων ασθενειών (πχ. διαβήτης, αναπνευστικές και εκφυλιστικές μυοσκελετικές παθήσεις, ψυχικές διαταραχές).27 Η ΑΤΥ θεωρείται χρήσιμο εργαλείο αντιμετώπισης του αυξανόμενου κόστους υπηρεσιών υγείας και σε πιο εξειδικευμένα θέματα (πχ. διασφάλιση επαρκών επιπέδων βιταμίνης D και πρόληψη-χειρισμός συμπτωμάτων κατάθλιψης με πολιτικές διαχείρισης ανεπαρκούς πρόσληψης βιταμίνης D).28
ΚΑΤΑΠΟΛΕΜΗΣΗ ΑΝΙΣΟΤΗΤΩΝ ΜΕΣΩ ΑΤΥ
Καταλυτικός είναι ο ρόλος της ΑΤΥ και στην αντιμετώπιση ανισοτήτων, μέσω ανασυγκρότησης του συστήματος υγείας, με ανακατανομή του ιατρικού προσωπικού για μεγιστοποίηση του κοινωνικού οφέλους, με ενίσχυση του θεσμού του οικογενειακού γιατρού, διαχωρισμό πρωτοβάθμιας, δευτεροβάθμιας και τριτοβάθμιας περίθαλψης (μείωση δαπανηρών εισαγωγών σε νοσοκομεία), καθολική υγειονομική κάλυψη (αποσύνδεση από το καθεστώς απασχόλησης), περιορισμός κατανάλωσης φαρμάκων και κόστους ευάλωτων πληθυσμών, ενθάρρυνση συμμετοχής πολιτών στη συναπόφαση διάθεσης πόρων, παρακολούθηση οικογενειακών προϋπολογισμών, θεσμοθέτηση ενός ελάχιστου βιοτικού επιπέδου, διεύρυνση του πλαισίου χορήγησης φοροαπαλλαγών-επιδομάτων-επιδοτήσεων, εφαρμογή σύγχρονων προγραμμάτων κοινωνικής προστασίας, μεταφορές πόρων σε ευάλωτες ομάδες (ενεργοποίηση δημοσιονομικού μηχανισμού στο πλαίσιο της κοινωνικής ισότητας, διανεμητική αποτελεσματικότητα και κοινωνική δικαιοσύνη, με στόχο την καταπολέμηση της φτώχειας με αντιμετώπιση του κοινωνικού αποκλεισμού), μέτρηση καταστροφικού κόστους υγείας-συσχέτιση με ανισότητες, αναβάθμιση προστασίας από οικονομικό κίνδυνο, ανάπτυξη προγραμμάτων προαγωγής ψυχικής υγείας και προώθηση ποιοτικών και οικονομικά προσιτών γενοσήμων εκδοχών πρωτότυπων φαρμάκων. Επίσης, με αποζημίωση φαρμάκων, βάσει σχέσης θεραπευτικού-οικονομικού οφέλους, τη συνεκδοχική απελευθέρωση δημοσιονομικού χώρου και τα εγχώρια συγκριτικά πλεονεκτήματα (αξιόπιστες παραγωγικές διαδικασίες, χαμηλότερο κόστος παραγωγής-διανομής), η Ελλάδα θα μπορούσε να αποτελέσει κέντρο παραγωγής αξιόπιστων γενοσήμων, με θετικό πρόσημο για τις οικονομικά ευάλωτες πληθυσμιακές ομάδες, διασφαλίζοντας απρόσκοπτη υγειονομική κάλυψη και προάσπιση της υγείας ως δημόσιου αγαθού.29
ΠΡΟΤΑΣΕΙΣ ΒΕΛΤΙΣΤΟΠΟΙΗΣΗΣ ΕΓΧΩΡΙΩΝ ΔΙΑΔΙΚΑΣΙΩΝ ΑΤΥ
Στο πανελλήνιο συνέδριο για τα οικονομικά και τις πολιτικές της υγείας (2023) και στο 8o συνέδριο ΑΤΥ (2023), παρουσία ειδικών σε Ελλάδα και Ευρώπη (εκπροσώπων πολιτικής ηγεσίας, θεσμικών φορέων, ακαδημαϊκών, στελεχών φαρμακευτικής αγοράς), ο συγγραφέας υπογράμμισε την ανάγκη ενσωμάτωσης στις διαδικασίες ΑΤΥ της ανάλυσης αποφάσεων πολλαπλών κριτηρίων σταθμισμένης βαρύτητας (Μulti-Criteria Decision Analysis-MCDA) που οδηγεί σε ανάπτυξη καλών πρακτικών MCDA (MCDA Emerging Good Practices) για έκδοση κατευθυντηρίων γραμμών, αποσαφήνισης της σημασίας της ΑΤΥ εντός του πλαισίου των κοινωνικών αρχών, συμπερίληψης όλων των ενδιαφερομένων με καθορισμό του ρόλου εκάστου εξ αυτών στις διαδικασίες ΑΤΥ (η συμμετοχή ασθενών και ιατρών θεωρείται εξόχως σημαντική προς εξασφάλιση αποδοχής του αποτελέσματος), αξιοποίησης (εν απουσία δεδομένων RCTs) του εκτεταμένου εγχωρίου ΣΗΣ και επικέντρωσης στην κλινική προστιθέμενη αξία, με υπολογισμό του πρόσθετου κόστους/μονάδα οφέλους υγείας (πχ. QUALY), αποκτώμενη από μία αξιολογούμενη υγειονομική παρέμβαση, συγκριτικά με την παρέμβαση αναφοράς, κατά το πρότυπο του HAS, που αξιολογεί τη συγκριτική βελτίωση του θεραπευτικού οφέλους, δια της παρεχομένης υγειονομικής υπηρεσίας (Amelioration du Service Medical Rendu-ASMR). Κάθε παρέμβαση με χαμηλό ICER εκτιμάται ευνοϊκή για αποφάσεις αποζημίωσης με ICER<όριο προθυμίας πληρωμής (Willingness To Pay-WTP) κοινωνίας-συστήματος υγείας (ήτοι του βαθμού στον οποίο η κοινωνία συσχετίζει το δημόσιο όφελος με αιτήματα-ανάγκες μεμονωμένων ασθενών εντός σταθερού προϋπολογισμού), οικονομικά αποδοτική και συνιστώμενη για εφαρμογή, ενώ τα φάρμακα με προστιθέμενη θεραπευτική αξία θα πρέπει να εντάσσονται άμεσα στον ΚΑΦ (Κατάλογο Αποζημιούμενων Φαρμάκων), επιταχύνοντας την πρόσβαση σε αυτά.
Παράλληλα, κατέθεσε συμπληρωματικές προτάσεις βελτιστοποίησης της λειτουργίας του εγχωρίου φορέα ΑΤΥ, όπως μείωση χρόνου αξιολόγησης-επίσπευση έγκρισης κυκλοφορίας υβριδικών φαρμάκων υψηλού κόστους και ορφανών φαρμάκων σπάνιων ασθενειών, επέκταση του πεδίου εφαρμογής με ενσωμάτωση ιατροτεχνολογικών προϊόντων και σκευασμάτων διατροφής για ειδικούς ιατρικούς σκοπούς, διεύρυνση της έκτασης του υπό μελέτη πληθυσμού στις κλινικές μελέτες, σχεδιαστική προσαρμογή-σύνδεση ΑΤΥ-EBM, αμεσότερη-έγκαιρη πρόσβαση ασθενών σε καινοτόμες θεραπείες (γονιδιακές-κυτταρικές για σπάνιες ασθένειες με χρήση του Next Generation Sequencing-NGS και Comprehensive Genomic Profile-CGP, ανάλυση γονιδιωματικού προφίλ με εξέταση βιοδεικτών) με προσιτό κόστος και μείωση χρόνου ολοκλήρωσης της διαδικασίας, καθορισμός δεοντολογικού πλαισίου, επένδυση σε επιστημονικό προσωπικό και ανάδειξη κοινωνικών ζητημάτων για ευρεία αποδοχή της διαδικασίας ΑΤΥ από όλους τους ενδιαφερόμενους.
ΣΥΜΠΕΡΑΣΜΑΤΑ
Σε εποχές δημοσιονομικών περιορισμών, η πολιτική υγείας οφείλει να υιοθετεί ολιστική προσέγγιση της αποδοτικότητας συστημάτων αξιολόγησης με επιτακτική την οικοδόμηση ισχυρού φορέα ΑΤΥ, ο οποίος συνεργαζόμενος με όλους τους ενδιαφερόμενους και συνεπικουρούμενος από την τεχνολογία, θα διασφαλίζει το μέγιστο όφελος για τη δημόσια υγεία και τους εκάστοτε εθνικούς οικονομικούς στόχους (αποσοβώντας ακροσφαλείς δημοσιονομικές αποφάσεις, με εξασφάλιση και ορθή κατανομή πόρων), την ανταγωνιστικότητα της βιομηχανίας και τη βιωσιμότητα του συστήματος υγείας, με παροχή εκσυγχρονισμένων υπηρεσιών, μέσω κοινωνικά δίκαιης, οικονομικά προσιτής και έγκαιρης πρόσβασης σε καινοτόμες θεραπείες.
ΒΙΒΛΙΟΓΡΑΦΙΑ
1. Μαλλιαρού Μ & Σαράφης Π. Οικονομική κρίση. Τρόπος επίδρασης στην υγεία των πολιτών και στα συστήματα υγείας. Το Βήμα του Ασκληπιού2012, 11:202–212
2. Morfonios Α, Kaitelidou D, Baltopoulos G, et al. The international practice of health technology assessment. Arch Hellen Med 2013, 30:19–34
3. Κιτρομηλίδου Χ. Αξιολόγηση τεχνολογίας υγείας & Συμφωνίες επιμερισμού κινδύνου. Εφαρμογή τους στο σύστημα υγείας της Κύπρου. Ανοιχτό Πανεπιστήμιο Κύπρου, Λατσιά, Λευκωσία, 2017
4. Turchetti G, Spadoni E, Geisler E. Health technology assessment. Εvaluation of biomedical innovative technologies. IEEE Eng Med Biol Mag 2010, 29:70–76
5. Μανιαδάκης Ν. Τα οικονομικά της Υγείας από την οπτική του μάνατζερ. Στο: Γραμματικοπούλου Ε (Επιμ.) Κοινωνία και υγεία IV. Εθνικό Ίδρυμα Ερευνών, Αθήνα, 2005:84
6. Kerr A, Todd C, Hebborn A, et al. A Comparison of international health technology assessment systems–Does the perfect system exist? Value Health 2014, 7: A441.
7. Neumann PJ. Lessons for Health Technology Assessment: It Is Not Only about the Evidence’, Value Health2009, 12(Suppl2):S45–S48.
8. Angelis A, Lange A, Kanavos P. ‘Using health technology assessment to assess the value of new medicines: Results of a systematic review and expert consultation across eight European countries’, Eur J Health Econ2018, 1:123–152.
9. O’Donnell JC, Pham SV, et al. Health technology assessment: lessons learned from around the world – an overview. Value Health2009, 12(Suppl2): S1-S5.
10. Lampe K, Pasternack I, Saarekas O, et al. Developing the HTA core model for the online environment. Int J Technol Assess Health Care 2014, 5:478-487.
11. Kaitelidou D, Katharaki M, Kalogeropoulou M, et al. The impact of economic crisis to hospital sector and the efficiency of Greek public hospitals. EJBSS 2016, 4:111-25.
12. Βαλιάνου Μ. Η Αξιολόγηση Τεχνολογίας Υγείας: Η διεθνής και ελληνική εμπειρία. Πανεπιστήμιο Πελοποννήσου, 2013
13. Raftery J, Roderick P, Stevens A. Potential use of routine databases in health technology assessment. Health technol assess2005, 9:1–92, iii–iv
14. Armataki E, Karampli E, Kyriopoulos J, et al. Health technology assessment of medicines in Greece: Pharmaceutical industry executives’ views. Int J Technol Assess Health Care 2014, 30:226-232.
15. Mentis Ι. The market of generic drugs in Southern Europe with the contribution of health technology assessment and competition. Arch Hellen Med 2021, 38: 89-94.
16. Kani C, Kourafalos V, Litsa P. Current environment for introducing health technology assessment in Greece. Int J Technol Assess Health Care2017, 33:396–401.
17. Garcia-Mochon L, Balbino JE, DE Labry Lima AO, et al. HTA and decision-making processes in Central, Eastern and Southeastern Europe: results from a survey. Health Policy2019, 123:182–190
18. Cheung KL, Evers SMAA, De Vries H, et al. Most important barriers and facilitators of HTA usage in decision-making in Europe. Expert review of Pharmacoeconomics & outcomes research, 2018, 18:297–304
19. Dias-Barbosa C & Hareendran A. Enhancing Patient Centricity of HTA Opportunities in Europe. Navigating the Path to Approval and Access, Evidera, London, 2019:39
20. Migliore A. Towards a regulation of HTA in Europe: the proposal from the European Commission. Expert Rev Med Devices 2019, 16:1–2
21. Vella Bonanno P, Bucsics A, Simoens S, et al. Proposal for a Regulation on Health Technology Assessment in Europe–opinions of policy makers, payers and academics from the field of HTA. Expert Rev Pharmacoecon Outcomes Res 2019, 19:251–261
22. Nachtnebel A, Mayer J, Erdos J, et al. HTA goes Europe: European collaboration on joint assessment and methodological issues becomes reality. Z Evid Fortbild Qual Gesundhwes 2015, 109:291–299
23. Makady A, Ten Ham R, De Boer A, et al. Policies for use of real-world data in health technology assessment (HTA): a comparative study of six HTA agencies. Value Health 2017, 20:520–532
24. Allen N, Liberti L, Walker SR, et al. A comparison of reimbursement recommendations by European HTA agencies: is there opportunity for further alignment? Front Pharmacol 2017, 8:384
25. Garattini L & Padula A. HTA for pharmaceuticals in Europe: will the mountain deliver a mouse? Eur J Health Econ 2020, 21:1–5
26. Mentis Ι. The introduction of Health Technology Assessment (HTA) in Greece and comparison with the European experience. Arch Hellen Med 2022, 39:313-321
27. Mentis Ι. Impact of health determinants on Greek health level, as capture of health production function. Arch Hellen Med 2024, 41:699-707
28. Mentis I. The effects of vitamin D on mood alteration in womenʼs life: Focus on depression. Acta Neurobiol. Exp. 2023, 83:307-316.
29. Mentis I. Impact of Health Indicators and Socio-Economic Inequalities on Greek Population’s Health Level in Relation to Causes. Acta Sci. Med. Sc 2022, 6.4: 03-12
ΔΙΑΔΙΚΤΥΑΚΟΙ ΤΟΠΟΙ
https://www.oloygeia.gr/health/politiki-ygeias/epitropi-ita/


